2024年のノーベル化学賞は、タンパク質の設計と構造予測を行ったワシントン大学(アメリカ)のデイビッド・ベイカー教授、グーグル・ディープマインド社(イギリス)のデミス・ハサビス博士(最高経営責任者)とジョン・ジャンパー博士(上席研究員)の3人に贈られました。彼らの功績について、情報理工学院の大上雅史准教授が解説します。大上准教授は、創薬などの視点に立ち、情報科学による分子デザインの研究を推進しており、今回のノーベル賞受賞研究についても日頃から興味を持っていたそうです。
2024年のノーベル化学賞の受賞理由を教えて下さい
大上
今年の受賞者は3名でしたが、受賞理由は大きく2つにわけられます。1つ目は、新しいタンパク質を計算によってつくったことです。これをタンパク質デザインと呼びますが、この業績によりベイカー先生が受賞しました。2つ目は、計算によってタンパク質のアミノ酸配列から構造を予測する研究で、こちらはハサビス博士とジャンパー博士の2名が受賞しました。
実は、ベイカー先生はタンパク質デザインだけではなく、タンパク質の構造予測にも長い間取り組まれてきました。一方で、ハサビス博士も構造予測だけでなく、タンパク質デザインのプログラムを開発しており、双方が受賞理由となった2つのポイントに関わる研究をしていた点が興味深いと感じました。また、ベイカー先生はワシントン大学の研究者ですが、グーグルのようなIT企業がこうした生命科学の研究を積極的に推進している点も非常に面白いと思います。

タンパク質の立体構造を予測することの意義を教えて下さい
大上
我々の体はタンパク質でできています。タンパク質は20種類のアミノ酸で構成されています。数十から数千個のアミノ酸が1本の長い鎖状になり、それが立体的に折りたたまれたとても複雑な構造をしています。たとえば、インフルエンザウイルスのあるタンパク質には独特のくぼみがあり、このくぼみに別の分子が結合することでウイルスの増殖が抑えられます。この仕組みを利用して開発されたのが、治療薬であるタミフルです。
このように、タンパク質の立体構造を知ることは、その働きを解明したり、新たな薬を開発したりする上で不可欠です。そのため、約40年前から、世界中の研究者が、X線結晶構造解析やクライオ電子顕微鏡法などの実験による方法でタンパク質の構造を計測してきました。しかし、タンパク質は何万種類もあるため、すべてのタンパク質の構造を調べるのは困難です。そこで1990年代に入り、コンピューターを使ったタンパク質の立体構造予測の研究が進められるようになりました。
今回のノーベル化学賞受賞について、まずは、ハサビス博士とジャンパー博士の功績を聞かせて下さい
大上
1990年代以降、コンピューターの急速な発展によりタンパク質の立体構造予測の研究が盛んになりましたが、当時の予測精度は低く、実用的ではありませんでした。そんな中、2018年にハサビス博士とジャンパー博士らが開発したのが、AlphaFoldというソフトウェアでした。
その後、2020年11月にはAlphaFold2が発表されました。彼らは、タンパク質の立体構造予測に関する国際的なコンペティション(CASP、キャスプ)でダントツの1位を獲得し、大きな注目を集めました。
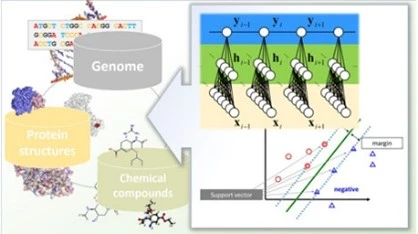
2021年7月に、AlphaFold2に関する論文がNature誌で公開されました。この論文で、AlphaFold2が、今回ノーベル物理学賞を受賞した人工ニューラルネットワークによる深層学習を活用していたことが明らかになりました。AlphaFold2の予測精度は90%を超えており、今後、創薬のスピードが大幅に向上することが期待されています。
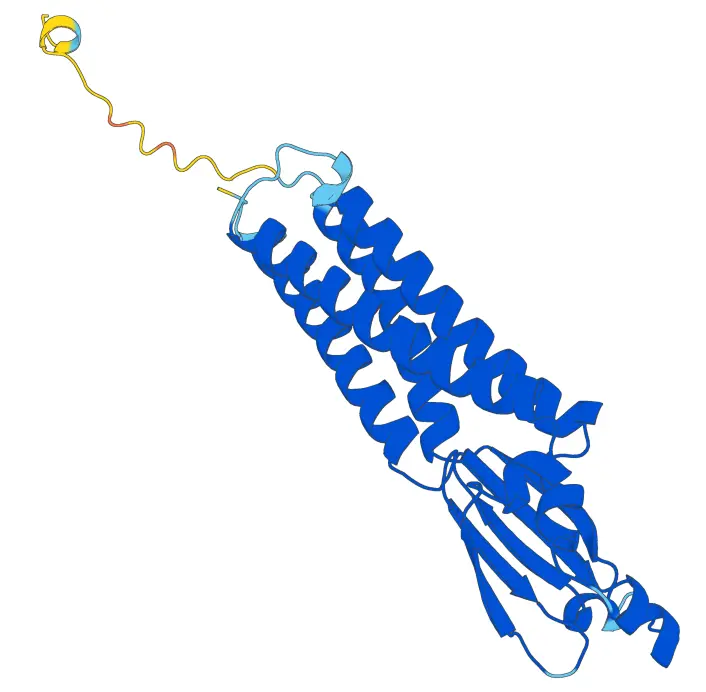
ヒトのClarin-2というタンパク質の予測構造。遺伝性難聴との関係が議論されていますが、まだ立体構造は明らかになっていません。
ベイカー先生の功績についても教えて下さい
大上
ベイカー先生も長年にわたり、コンピューターを使ったタンパク質の立体構造予測に取り組んできた研究者ですが、今回の受賞理由はタンパク質デザインです。その研究について順を追って説明しましょう。
基本的に、タンパク質の立体構造はエネルギー的に一番低い状態で安定すること、また、アミノ酸の配列が似ていれば立体構造も似ることがわかっていました。この知見をもとに、ベイカー先生は自然界には存在しない、まったく新しいタンパク質の立体構造を2003年に設計しました。ベイカー先生らも立体構造予測を行うソフトウェアであるRosettaを開発していましたが、Rosettaを転用して、構造予測とは逆にタンパク質の立体構造を与えると、エネルギー的に安定するようなアミノ酸の配列を割り出すことができるようにしたのです。
さらに、ベイカー先生は、割り出されたアミノ酸の配列をもとに、実際に微生物にタンパク質を作らせて、その構造を調べました。このときにデザインされたタンパク質は「Top7」と名付けられており、93個のアミノ酸からできていました。微生物が作り出したTop7は、ベイカー先生が設計したとおりの立体構造をしていました。この研究成果は2003年に発表され、世界中の研究者を驚かせました。当時、Top7は人工的に作られたタンパク質の中では最大のものであり、なにより似た配列のタンパク質が存在していないにも関わらず狙ったとおりの構造を作れていたからです。現在のところ、タンパク質の働きと立体構造との関係はまだよくわかっていませんが、今後、研究が進めば、新しい機能をもつ新たな生命体をもデザインすることも可能になるかもしれません。
大上先生の研究テーマは、「情報科学によるライフイノベーション」とのことですが、現在どのような研究に取り組まれているのでしょうか
大上
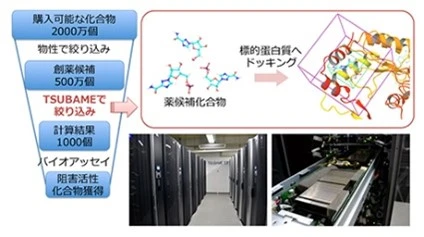
新型コロナ感染症の報道で、抗原や抗体という言葉をよく耳にしたと思います。抗原や抗体はいずれもタンパク質でできています。新型コロナウイルスなどの抗原が体内に侵入した際、その抗原のみと結合するように設計されたものが抗体医薬です。我々の研究室でも、RosettaやAlphaFold2を使い、狙った抗原のみと高効率に結合する抗体医薬品の開発に向けた研究を進めています。
東京科学大学には、AI予測を可能にする高性能なスーパーコンピューター TSUBAME 4.0があり、大規模な計算が可能です。また、タンパク質の立体構造予測に関する研究者も数多くいます。これらの環境を最大限に活用し、情報交換や共同研究を通じて、医学や化学、生命科学の発展に情報理工学の立場から貢献していきたいと考えています。

*本記事は、2024年11月20日(水)にオンライン開催されたScience Tokyoノーベル賞解説講演会の内容をもとに制作しています。
大上准教授の研究をもっと詳しく知るには
東京科学大学で行われている類似の研究
「2024年ノーベル賞を読み解く」シリーズ
お問い合わせ
研究支援窓口