胎児の成長において必要不可欠な胎盤。さまざまな機能を持つ重要な臓器だが、現在、医療や創薬分野が注目するのは、胎児を外部の有害物質やウイルスから保護するバリア機能だ。胎盤に無数にある絨毛がフィルターのような働きをし、有害な物質から胎児を守る。ただし、全てを防げるわけではない。ニコチンやカフェインなどを妊娠中に控えるのは、分子量が小さく、フィルターを通過して胎児に移行してしまうからだ。また、一部の医薬品やウイルスも胎盤を透過し、胎児に影響を及ぼすことが知られている。医薬品を開発する上では、物質の胎盤透過性や胎児への移行量を正確に把握することが必要なのである。
しかしながら胎盤は「研究が最も遅れている臓器」と呼ばれるほど謎が多い臓器で、胎盤透過のメカニズムは未解明な部分が大きい。研究が遅れているのは、動物種によって構造が大幅に異なり、動物実験から得られたデータを人間に当てはめることが困難だからだ。動物実験では異常が見られなかった医薬品を妊娠中の女性が服用したところ、子どもに先天性の形態異常が現れたケースが報告されたこともある。また、健康で欠損のない人間の胎盤を入手することが難しく、正確な実験ができないことも研究の遅れにつながっているようだ。
胎盤透過性メカニズムの解明に向けて道筋を照らしたのが、生体材料工学研究所の梶弘和教授である。医療工学を専門とする彼は、東北大学医学系研究科が樹立したヒト胎盤幹細胞から胎盤オルガノイドを生成し、シート状の胎盤バリアモデルを再現することに成功した。これにより、物質の胎盤透過性が定量的に推定可能となり、より適切な医療措置や胎児への副作用を最小限にした医薬品開発に役立てられると期待されている。このモデルによる安全性のテストが動物実験の代替となるため、倫理的な問題の解決や、医薬品の開発スピードの向上にも貢献するだろう。その他にも、胎盤の形成メカニズムや妊娠中の疾患といった幅広い研究分野でも活用が見込まれている。未来の胎盤研究を照らす新たな技術について、梶教授に話を伺った。
ピックアップ
胎児の成長を支える胎盤
母体と胎児を連絡する臓器。内部の血管を通じて胎児に栄養や酸素などを供給するほか、胎児が排出した老廃物を授受するなど、胎児の成長において重要な役割を担う。
有害物質を防ぐバリア機能
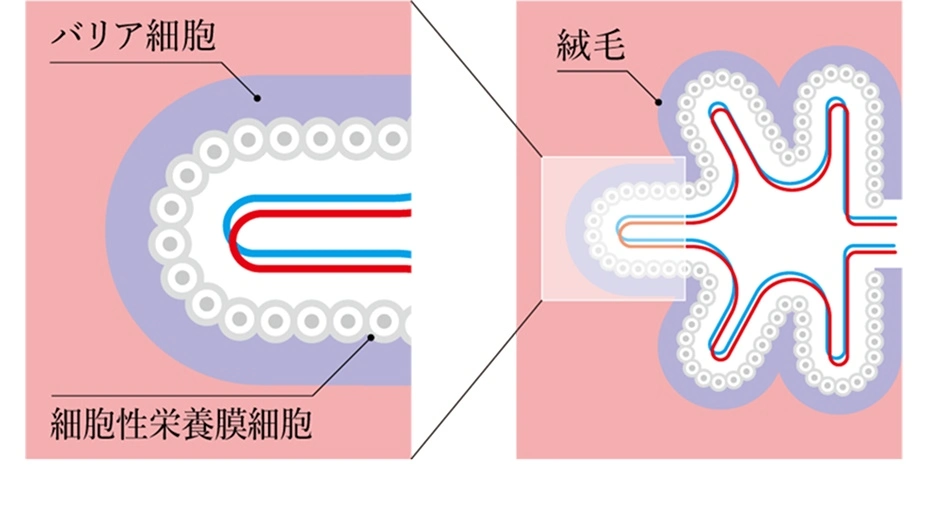
母体から胎児へ物質が送られる中で、胎児にとって悪影響を及ぼすものは除外される。胎盤内に密生している絨毛(じゅうもう)はバリア細胞(合胞体性栄養膜細胞)と細胞性栄養膜細胞で覆われており、バリア細胞がフィルターとなる。
胎盤と胎児をつなぐ臍帯(さいたい)
胎盤内の血液を胎児に送り、老廃物を胎盤に送るためのひも状の器官。
“最も研究が遅れている臓器の一つ、胎盤。
胎盤バリアモデルがその謎に挑戦する鍵となるでしょう”

バリア機能の再現は試行錯誤の連続。研究を重ね、ついに実用的なモデルが完成した
生体外で幹細胞[用語1]を培養し、臓器を再現した3次元組織をオルガノイドと呼びます。臓器の複雑な構造を知ることができるため、医学や生物学、薬学などの分野で役立てられています。胎盤研究においては、ヒト胎盤幹細胞(ヒトTS細胞)が長らく樹立されておらず、絨毛癌細胞から作られるモデルしかありませんでした。健康な組織ではないため、データの正確性に乏しいという欠点があったのです。そんな中飛び込んできたのは、長らく研究を共にしている東北大学医学系研究科の研究チームが、ヒト胎盤幹細胞の樹立に成功したというニュース。研究仲間から、この幹細胞が何か研究に役立てられないかと相談を受け、母体や胎児の健康に直結する胎盤のバリア機能解明を目指し、絨毛構造を再現したヒト胎盤オルガノイドの開発に着手しました。
一筋縄では行かないのが研究の世界。一般的にオルガノイドを作製する際に使われるマトリゲルという細胞の足場を使用したところ、バリア細胞が内側、未分化の胎盤幹細胞が外側という実際の絨毛とは逆の構造になると判明しました。表裏を反対にするために試行錯誤したところ、アガロースのマイクロウェル(小さなくぼみのあるプレート)が効果的であると発見。それを用いて8日間培養した結果、バリア細胞が外側、未分化幹細胞が内側となる球体のオルガノイドがついに完成しました。完成したオルガノイドは、実際の絨毛と同様に表面の細胞が融合していたことも観察されました。
オルガノイドが完成したとはいえ、まだゴール達成ではありません。今回の目的は、胎盤の物質透過性を測ることですが、球体のオルガノイドでは物質の透過性の評価をしづらいという欠点がありました。球体のままでは、どの物質がどれほど絨毛を透過したかの定量的な評価に不向きだったのです。そこで胎盤オルガノイドの生成条件を応用し、シート状の胎盤バリアモデルの開発に着手。コラーゲンの膜に幹細胞を培養することで平面状のオルガノイドが生成されると分かり、シートの広範囲でバリア細胞と未分化の胎盤幹細胞の2層構造を再現することに成功しました。
本モデルの使い方は簡単です。シートの下部に溶液を配置し、溶質がどれほどシートの上部に移行したかを測ることで、物質の透過具合を調べることができます。検証すると、すでに透過性が認められている物質についても、実物の胎盤と同様の傾向を示しました。
このモデルは早くも多方面から問い合わせを受け、研究に役立てられています。特に創薬や食品開発の分野においては、新薬や食品の安全性評価のための活用が見込まれています。動物実験に代わり本モデルで医薬品やサプリメントの安全性を調べることで、人間の胎盤を想定したデータが得られるほか、検証期間の短縮につながります。将来的には、本モデルでマタニティサプリメントに認証を与える、といった仕組みを構築したいと考えています。
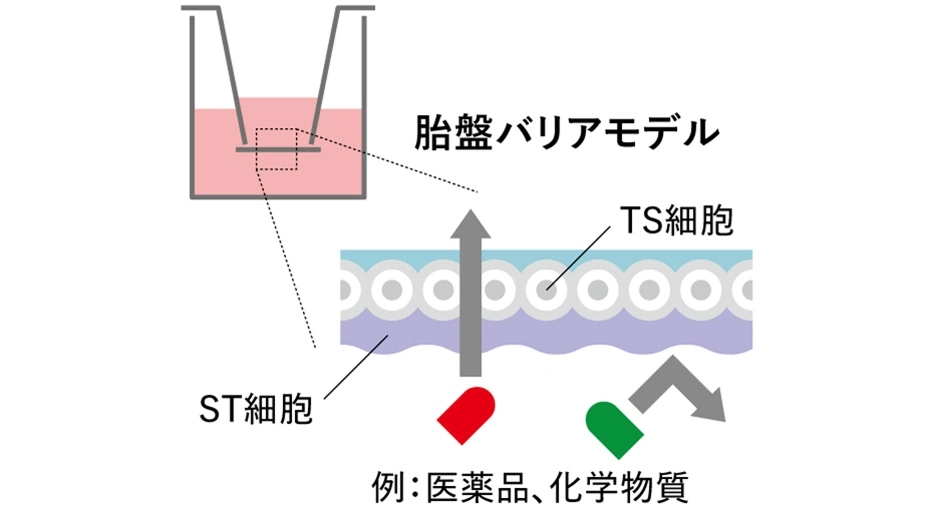
シート状の胎盤バリアモデルを用いた物質透過性の評価方法
2層構造のうち、下部のバリア細胞(ST細胞)がフィルターとなり、医薬品や病原菌の透過を左右する。ブロックされたものはシートの下部へ、透過したものは上部へと移行する。
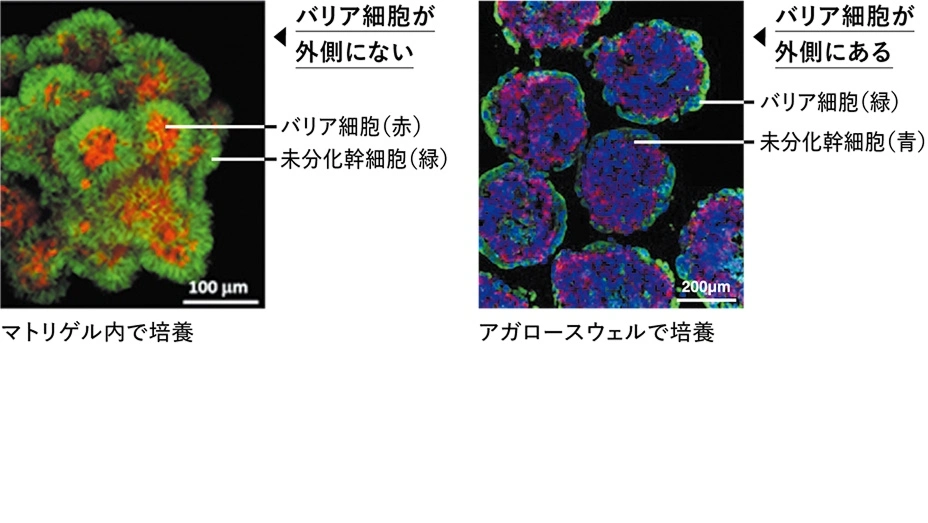
マトリゲルとアガロース、それぞれで培養した胎盤オルガノイド
左はマトリゲルで培養した胎盤オルガノイドの写真。本来外側にあるべきバリア細胞が内側に隠れ、正しい構造とは反対になっていると分かる。右はアガロースで培養した胎盤オルガノイドを半分に切片した写真。正常な胎盤絨毛と同じように、外側にバリア細胞が集合している。
“「面白そう」という好奇心を頼りに自由な発想で研究をデザインする。常に目指すは医療と研究の発展”
生体由来の材料(バイオ材料)が貢献する医療・研究の未来
私の研究室では生体由来の材料(バイオ材料)を用いたマイクロ・ナノ技術を基盤とし、胎盤オルガノイドのような生体模倣システム[用語2]や体内埋め込み型デバイス、細胞デリバリーシステムといった医療工学の研究を進めています。例えば、後眼部疾患用のドラッグデリバリーデバイス。薬を含んだ小さな装置を、目薬が届かないような眼の奥部分に貼り付けると、少量ずつ継続的に患部へ投薬され、患者さんの負担を緩和することができます。
昨今では移植医療やバイオ医薬品など生体に関わる研究が進化を続けています。従来のプロダクトでは対応できない医療分野も増えており、新たなバイオマテリアル技術でその一助となることが研究の目的です。
連携の幅は無限大。斬新な発想で人に役立つ技術を生み出す
医療工学と出会ったのは大学の博士課程時代、アメリカのマサチューセッツ工科大学(MIT)に留学した時のことです。もともとは物理化学を専攻していましたが、組織・臓器の体外生成研究の提唱者、ロバート・ランガー氏の門下に入り、当時注目を集めていたバイオマテリアルの研究に引き込まれていきました。天才的なロバートの周囲には個性豊かな学生や研究者が数多く集まり、「こんな発想をする人がいるのか」と世界の広さを知った経験でした。
若い時に得た視野の広さは今の柔軟な姿勢にも生きていて、できるだけ多様な研究分野と連携し、技術で貢献したいと考えています。「面白そう」と思った道に迷わず進む。そのフットワークの軽さが他分野の研究者とのつながりを生み、連携の幅を広げています。それぞれの分野に対して、ある意味素人の感覚で関わるので、専門家は思いつかないような斬新な発想ができるのかもしれません。東京工業大学と東京医科歯科大学の統合により、医工連携がより加速するのではないかと期待しています。医療工学の技術で研究や治療の前進に貢献し、一人でも多くの患者さんの役に立てるよう、今後も研究を続けていきます。
用語説明
- [用語1]
- 幹細胞:細胞の再生や生産に関わる細胞。自分と同じ性質の細胞を複製する自己複製能や、体内のいろいろな細胞に分化する能力などを持つ。胎盤由来の幹細胞は胎盤幹細胞(TS細胞)と呼ばれ、自己複製と胎盤を構成する細胞への分化を行うことができる。
- [用語2]
- 生体模倣システム:臓器の機能を再現したオルガノイドや臓器チップなど、生物の細胞を体外において人工的に3次元で培養したもの。薬剤の効果や副作用の評価、病気のメカニズムや生体機能の解明など幅広いシーンで役立てられている。
My future research
世界初の胎盤バリアモデルを提供し、胎盤研究界での存在感を高める
今回開発した胎盤バリアモデルの活用推進を目指し、2023年に株式会社HPSというベンチャー企業を立ち上げました。胎盤バリアモデルを企業や研究機関に提供し、医薬品や機能性食品の胎盤透過性の評価に役立ててもらおうと考えています。定量的な評価に用いられる胎盤バリアモデルは世界初で、将来的には「胎盤透過性の評価といえば日本」といわれる未来があるもしれません。このモデルに限らず、生体デバイスは利用されて初めて意義があります。デバイスのメリットを発信し、技術普及に努めていきたいです。
プロフィール
梶弘和(Hirokazu Kaji)
総合研究院 生体材料工学研究所 教授

2005年、東北大学大学院工学研究科バイオロボティクス専攻博士課程修了。2009年、日本学術振興会海外特別研究員、2011年、東北大学工学研究科准教授を経て、2021年より東京医科歯科大学(現・東京科学大学)生体材料工学研究所教授。株式会社HPS取締役CTO。
関連リンク
取材日:2024年11月21日/駿河台キャンパスにて
更新履歴
- 2025年10月21日 タイトルの編集を行いました。
